| BG | CS | DA | DE | EL | EN | ES | ET | FI | FR | HU | IT | LT | LV | MT | NL | PL | PT | RO | SK | SL | SV |
Skema til opfyldelse af datakrav
Bilag VI i REACH-forordningen beskriver et generelt skema med 4 trin, der skal følges af producent og importør1 til opfyldelse af oplysningskravene ved registrering:
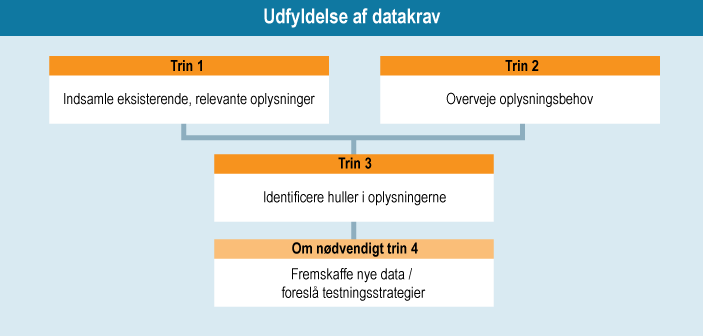
Trin til indsamling af oplysninger
Alle eksisterende data vedrørende de iboende egenskaber ved stoffet, der skal registreres, bør indsamles uden hensyntagen til mængden: Oplysninger om effekter på mennesker, testdata (fysisk-kemisk data, in vitro-data og in vivo-data) og ikke-testdata (data opnået med prædiktive redskaber). Eksponeringsdata bør også indsamles for at få indsigt i de eksponerede befolkningsgrupper og afdelinger samt eksponeringernes natur, dvs. vej, frekvens og varighed.
Sådanne oplysninger kan skaffes fra forskellige kilder så som virksomheders interne data, fra andre producenter og importører (hvis der er en aftale om samarbejde på dette trin) eller fra databaser og andre litteraturkilder. Indhentning af resultater fra ikke-forsøgsmetoder vil især være vigtig ved stoffer, hvor testdata er begrænsede eller ikke-eksisterende.
De indsamlede oplysninger om de fysisk-kemiske egenskaber og dets skæbne i miljøet, stoffets toksicitet og økotoksicitet bør bedømmes ud fra deres pålidelighed, relevans og fuldkommenhed2.
Overvejelser om oplysningsbehov
Oplysningskrav afhængig af mængde i REACH om fysisk-kemiske, toksikologiske og økotoksikologiske egenskaber bliver beskrevet i kolonne 1 i bilagene VII og X. Specifikke regler for tilpasning bliver opgivet i kolonne 2 på disse bilag, hvorimod generelle regler for tilpasning af disse standardkrav kan findes i bilag XI. For stoffer, der fremstilles og importeres i mængder imellem 1 og 10 tons om året, skal der kun fremskaffes oplysningskrav om toksikologiske og økotoksikologiske egenskaber for alle "ikke-fasningsstoffer"3 og for "fasningsstoffer"4, der opfylder de farekriterier, der er forskrevet i REACHs bilag III.
Identifikation af manglende oplysningerne
Der må foretages en bedømmelse af de tilgængelige oplysningers tilstrækkelighed for at kunne drage konklusioner om risikobedømmelse, dvs.:
- afgøre, om stoffet skal klassificeres, i fald ja, definer klassificering og etikettering.
For stoffer ≥ 10 tons om året,
- afgøre, om stoffet er persistent, bioakkumulerende og giftigt (PBT) eller meget persistent og meget bioakkumulerende (vPvB),
- identificere (en) dosisdeskriptor(e), der muliggør udledning af (en) koncentration(er) af stoffet under hvilke(n) uønskede bivirkninger i den implicerede miljøsfære ikke forventes at forekomme [PNEC(’er), forventet nuleffektkoncentation(er)],
- identificere (en) dosisdeskriptor(e), der muliggør udledning af (et) niveau(er) af eksponering af stoffer over hvilke(n) en gruppe mennesker ikke bør eksponeres [DNEL(’er)5 udledt(e) nuleffektniveau(er)].
Anses de tilgængelige oplysninger for utilstrækkelige ved mindst et af de ovenstående punkter, er der brug for yderligere oplysninger til at udfylde manglende data i bilagene VI til X.
Fremskaffelse af nye oplysninger eller forslag til testningsstrategier
Når der er huller i oplysningerne, der ikke kan udfyldes med ikke-forsøgsmetoder, bliver potentielle registranter nødt til at skride til handling afhængig af de manglende forsøg/oplysninger:
- anvendes bilagene VII og VIII, skal registranten fremskaffe nye oplysninger,
- anvendes bilagene IX og X, skal registranten forberede et forslag til forsøg og indsende det til bedømmelse som del af registreringsdossieret til Europæisk Kemikalieagentur.
Forsøg på hvirveldyr skal altid være den sidste udvej.
Det må bemærkes, at REACH har adskillige forordninger til at muliggøre datadeling mellem registranter. Data, der er indhentet ved forsøg på hvirveldyr, skal deles (mod betaling).
Rammer for generel beslutningstagen (GDMFGDMF’er) er blevet udviklet i Guidance on information requirements and chemical safety assessment. De uddyber de procedurer, som registranten skal følge i trin 1 til 4. GDMF’er er illustreret i de følgende skematiske diagrammer:
- Stoffer, der bliver fremstillet eller importeret i kvantiteter mellem 1 og 10 tons om året,
- Stoffer, der bliver fremstillet eller importeret i mængdeintervallet ≥ 10 ton om året.
1. Producenter uden for EU kan udpege "enerepræsentanter" til at opfylde importørernes forpligtelser. Enerepræsentanter er fysiske eller juridiske personer, der er etableret i den Europæiske Union og som har tilstrækkelig baggrundsviden om praktisk håndtering af stoffer og oplysninger i relation til disse. Når en enerepræsentant er udpeget, har producenten uden for EU pligt til at informere importøren(rne) inden for den samme leverandørkæde om udnævnelsen. Efter denne kommunikation indtager enepræsentanten EU-importørernes rolle og opfylder disses registreringsforpligtelser.
2. Pålidelighed: En forsøgsrapport eller udgivelses iboende kvalitet. Datapålidelighed er tæt forbundet med pålideligheden af den forsøgsmetode, der er anvendt til at fremskaffe data. Relevans: Graden af hvordan data og forsøg er egnet til særlig identifikation af fare eller karakterisering af risiko.
3. Ikke-indfasningsstoffer: Stoffer, der ikke opfylder definitionen for indfasningsstoffer som givet i forordningen.
4. Et "indfasningsstof" er et stof, der allerede under visse betingelser fremstilles eller importeres før ikrafttrædelsen af REACH den 1. juni 2007 (artikel 3(20). I REACH-forordningen gives der den nøjagtige definition af et "indfasningsstof").
5. Det er ikke altid muligt at etablere et kvantitativt DNEL via identifikation af en konkret kvantitativ værdi af dosisdeskriptoren. I de situationer er det dog muligt at definere nogle kvantitative og semikvantative dosisdeskriptorer eller en kvalitativ fremgangsmåde, der også ville kunne muliggøre en konklusion om, at stoffets anvendelse og håndtering anses for at være kontrolleret på en fyldestgørende måde.
|
Prévention du risque chimique, Frankrig, 2007 |

