| BG | CS | DA | DE | EL | EN | ES | ET | FI | FR | HU | IT | LT | LV | MT | NL | PL | PT | RO | SK | SL | SV |
Schema de îndeplinire a cerinţelor informaţionale
Anexa VI a regulamentului REACH descrie schema generală alcătuită din cei patru paşi de urmat de către producător sau importator1 pentru îndeplinirea cerinţelor informaţionale legate de înregistrare.
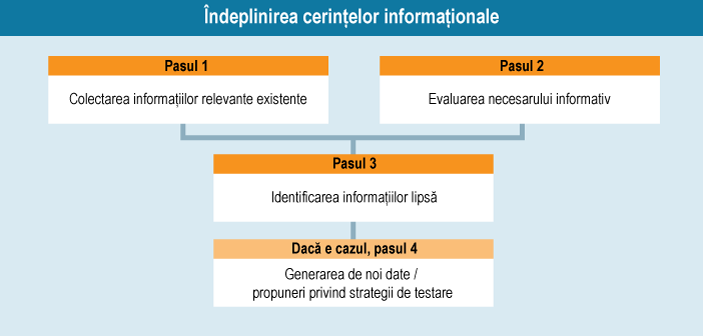
Etapa colectării informaţiilor
Trebuie colectate toate datele existente cu privire la proprietăţile intrinseci ale substanţei de înregistrat, indiferent de tonaj: datele antropologice, datele de pe urma testării (datele fizico-chimice, datele in vitro şi in vivo) şi datele obţinute cu ajutorul metodelor de predicţie. Trebuie colectate de asemenea şi informaţii privitoare la expunere, pentru a înţelege care sunt populaţiile şi domeniile expuse, precum şi natura expunerilor, adică ruta, frecvenţa şi durata.
Aceste informaţii pot fi obţinute dintr-o varietate de surse, cum ar fi informaţiile interne ale companiilor, de la alţi producători sau importatori (dacă există un acord privind cooperarea în această etapă), din bazele de date sau din alte surse din literatura de specialitate. În cazul substanţelor pentru care datele de pe urma testării sunt limitate sau inexistente, este extrem de importantă obţinerea de rezultate din metode care nu implică testarea.
Informaţiile referitoare la proprietăţile fizico-chimice şi de evoluţie în mediul înconjurător, la toxicitatea şi ecotoxicitatea substanţei trebuie evaluate din punctul de vedere al corectitudinii, relevanţei şi completitudinii2.
Evaluarea necesarului informaţional
Cerinţele informaţionale pe grupe de tonaj din regulamentul REACH în ceea ce priveşte proprietăţile fizico-chimice, toxicologice şi ecotoxicologice sunt descrise în coloana 1 a anexelor de la VII la X. În coloana 2 a acestor anexe sunt prezentate regulile specifice de adaptare, iar regulile generale de adaptare a acestor cerinţe standard sunt prezentate în anexa XI. În cazul substanţelor produse sau importate în cantităţi între 1 şi 10 tone pe an, cerinţele informaţionale privitoare la proprietăţile toxicologixe şi ecotoxicologie trebuie specificate numai pentru toate „substanţele neintroduse”3, precum şi pentru “substanţele în curs de introducere”4 care îndeplinesc criteriile de risc precizate în anexa III a regulamentului REACH.
Identificarea informaţiilor lipsă
Trebuie apreciat dacă informaţiile disponibile sunt adecvate pentru a putea emite concluzii referitoare la evaluarea riscurilor, astfel:
- se va determina dacă substanţa trebuie clasificată, în caz afirmativ se va defini clasificarea şi etichetarea.
Pentru substanţe ≥ 10 tone pe an,
- se va determina dacă substanţa este persistentă, bioacumulantă şi toxică (PBT), sau foarte persistentă şi foarte bioacumulantă (fPfB),
- se vor idenfica descriptori de dozaj care să permită derivarea unor concentraţii ale substanţei sub nivelul cărora nu se aşteaptă efecte negative asupra mediului de interes [CTNE, Concentraţii Teoretice de Non-Efect],
- se vor identifica descriptori de dozaj care să permită derivarea unor niveluri de expunere la substanţă peste care grupurile umane trebuie să evite expunerea [NDNE5, Niveluri Derivate de Non-Efect].
Dacă informaţia disponibilă este considerată a fi inadecvată cel puţin unuia dintre obiectivele de mai sus, sunt necesare informaţii suplimentare pentru a completa omisiunile de pe anexele VII – X.
Generearea de noi informaţii sau propunerea de strategii de testare
Atunci când lipsesc informaţii ce nu pot fi completate prin metode neexperimentale, potenţialii declaranţi trebuie să acţioneze în funcţie de testul/informaţia lipsă:
- în cazul în care se aplică anexele VII şi VIII, declarantul trebuie să genereze noi date,
- în cazul în care se aplică anexele IX şi X, declarantul trebuie să pregătească o propunere de testare şi să o prezinte Agenţiei Europene pentru Substanţe Chimice odată cu dosarul de înregistrare.
Testarea pe vertebrate trebuie să reprezinte soluţia ultimă.
Trebuie reţinut că regulamentul REACH are mai multe prevederi care facilitează partajarea datelor între declaranţi. Datele obţinute în urma testării pe vertebrate trebuie partajate (contra cost).
În cadrul Guidance on information requirements and chemical safety assessment, au fost create Scheme Generale pentru Luarea Deciziilor (SGLD). Acestea aprofundează procedurile ce trebuie urmate de către declarant în paşii de la 1 la 4. SGLD sunt ilustrate în următoarele diagrame:
- Substanţe produse sau importate în canităţi între 1 şi 10 tone pe an,
- Substanţe produse sau importate în canităţi ≥ 10 tone pe an.
1. Producătorii non-UE pot numi “Reprezentanţi unici" pentru a îndeplini obligaţiile importatorilor. Reprezentanţii unici sunt persoane fizice sau juridice stabilite în Uniunea Europeană şi care au o experienţă suficientă privind manipularea practică a substanţelor şi informaţiile referitoare la ele. Atunci când este numit un Reprezentant unic, producătorul non-UE are obligaţia de a notifica importatorul (importatorii) din cadrul aceluiaşi lanţ de aprovizionare, despre numirea respectivă. În urma acestei notificări, Reprezentantul unic preia rolul importatorilor UE şi îndeplineşte obligaţiile acestora privind înregistrarea.
2. Corectitudinea: calitatea inerentă a unui raport de test sau a unei lucrări. Corectitudinea datelor este strâns legată de corectitudinea metodei de testare utilizate pentru generarea lor. Relevanţa: măsura în care datele şi testele sunt adecvate pentru identificarea sau caracterizarea unui anumit risc.
3. Substanţe neintroduse: substanţe care nu respectă definiţia substanţelor în curs de introducere, aşa cum este ea expusă în regulament.
4. O “substanţă în curs de introducere” este o substanţă deja produsă sau importată, în anumite condiţii, înainte de intrarea în vigoare a regulamentului REACH la 1 iunie 2007 (articolul 3(20) din regulamentul REACH oferă definiţa exactă a unei substanţe “în curs de introducere”).
5. Nu este întotdeauna posibilă stabilirea unui NDNE cantitativ prin intermediul identificării unei valori cantitative concrete a descriptorului de dozaj. În aceste situaţii, există totuşi posibilitatea de a defini un anumit descriptor cantitativ sau semi-cantitativ de dozaj, sau posibilitatea unei abordări calitative care să ducă la concluzia că utilizarea şi manipularea substanţei pot fi considerate sub control.
|
Prévention du risque chimique, Franţa, 2007 |

